تمكَّن الباحثون من البرهنة على الأهمية المحتملة للعُضيَّات المستزرَعة مخبريًا في دراسة العقاقير الجديدة المضادة للفيروسات، غير أن أبحاثهم لم تُسفر بعدُ عن علاجات يمكن طرحها في الأسواق. حتى الآن، يمكن القول إنَّ تقنية العُضيَّات قد استفادت من الجائحة، أكثر مما أفادت في تطوير علاجات لهذا المرض...
بقلم: سمريتي مالاباتي
فريقٌ من علماء الفيروسات يحقن ملايين العضيَّات المستزرَعة مخبريًا (وهي نماذج مُصغَّرة للأعضاء البشرية) بفيروس «سارس-كوف-2»، بهدف التعرُّف على الكيفية التي يُدمِّر بها الفيروس أعضاء الجسم، وكيفية التصدي له.
أمضت شويبنج شين قرابة الشهرين في العناية بنحو نصف مليون رئة مصغَّرة، تبدو الواحدة منها أشبه بسحابةٍ قاتمة متناهية الصغر، قابعة داخل طبق دافئ، تحميها قبةٌ من الهلام. كانت شين، وهي اختصاصية بيولوجيا الخلايا الجذعية بكلية وايل كورنيل للطب في مدينة نيويورك، قد استنبتت – بمعاونة فريقها – هذه الرئات المصغَّرة من مجموعات من خلايا بشرية، وكانت تمدُّها بالمواد المغذية كل بضعة أيام خلال نموها، لتتخذ شكل أكياس هوائية ثلاثية الأبعاد.
وقد اكتمل نمو تلك «العُضيَّات المستزرَعة مخبريًا» oragnoids، لتصير الواحدة منها في حجم حبة العدس. بعد ذلك، جمعها الفريق، ونقلها إلى مختبر قريب، مُصرَّح له بالتعامل مع فيروس «سارس-كوف-2»، وهو الفيروس المسبِّب لجائحة «كوفيد-19». في هذا المختبر، غُمرت الرئات المصغَّرة بالفيروس، ثم غُمر كل منها في عقار واحد، من بين 15 ألف عقار، فأدَّى ذلك إلى تَلَف جميع الرئات المصغَّرة تقريبًا. غير أن بضعة عقاقير تمكَّنت من وقف انتشار العدوى، واعتُبرت تلك العقاقير علاجاتٍ محتمَلة لمرض «كوفيد-19».
تُعَد شين واحدة من قائمةٍ طويلة من علماء البيولوجيا الخلوية الذين دفعتهم الجائحة إلى التوسُّع في الاعتماد على تقنية استزراع العُضيَّات مخبريًا من أجل دراسة الأمراض المُعدية. ففي العام الماضي، طوَّر الباحثون نماذج مصغَّرة لأعضاء مثل الرئة، والأمعاء، والكبد، والدماغ، وغيرها كثير، لاستجلاء الكيفية التي يصيب بها فيروس «سارس-كوف-2» هذه الأعضاء؛ وهو ما مكّنهم من تحديد الخلايا التي يستهدفها الفيروس في هجومه، وسرعة الهجوم، وطبيعة الاستجابة التي تصدر عن الخلايا حيال ذلك الهجوم.
يقول هانز كليفرز، اختصاصي البيولوجيا التطورية في معهد أوبريخت، في مدينة أوتريخت الهولندية: "أصبحت العُضيّات المستزرَعة أداةً مهمة من الأدوات التي يستعين بها علماء الفيروسات في أبحاثهم". فيما مضى، استُخدمت هذه التقنية بصفةٍ أساسية لدراسة علم البيولوجية البشرية الأساسية، فضلًا عن دراسات النمو وما يتصل به من اضطرابات، وكذلك الأمراض السرطانية. في تلك المرحلة، لم يُقدِم على استخدام تلك النماذج لدراسة الفيروسات والأمراض المُعدية سوى عددٍ قليلٍ من المختبرات. لكن كليفرز يرى أن الجائحة وضعت العُضيَّات في دائرة الضوء، ودفعَتْ العلماء إلى إجراء أبحاث عالية التأثير، كما أثبتت أهميتها في إنتاج العقاقير.
وترجع أهمية العُضيَّات المستزرعة إلى أن النُّهُج المتبَّعة حاليًّا في دراسة الفيروسات تشوبها أوجه قصور عدَّة. فالركيزة الأساسية التي طالما استند عليها علم الفيروسات هي سلالة من الخلايا السرطانية، عَزَلَها الباحثون من كُلى السعدان الأخضر الأفريقي Chlorocebus sabaeus للمرة الأولى قبل 60 عامًا، ولا تزال تواصل انقسامها منذ ذلك الحين. هذه الخلايا، المعروفة باسم «خلايا فيرو» Vero cells، تمثل وسطًا ممتازًا لزراعة الفيروسات، إلا أنها لا تعكس استجابة الجسم البشري الطبيعية لهذه الفيروسات. تقول إلكا مولبرجر، عالمة الفيروسات في جامعة بوسطن بولاية ماساتشوستس، إن تلك الخلايا "لا تُجدي نفعًا في حقيقة الأمر". ويستعين الباحثون أيضًا ببعض سلالات الخلايا السرطانية البشرية، لكن، كما هو الحال مع خلايا فيرو، لا تستجيب هذه الخلايا للعدوى الفيروسية بنفس الطريقة التي تستجيب بها الخلايا الطبيعية.
تمكَّن الباحثون من البرهنة على الأهمية المحتملة للعُضيَّات المستزرَعة مخبريًا في دراسة العقاقير الجديدة المضادة للفيروسات، غير أن أبحاثهم لم تُسفر بعدُ عن علاجات يمكن طرحها في الأسواق. يقول كليفرز: "حتى الآن، يمكن القول إنَّ تقنية العُضيَّات قد استفادت من الجائحة، أكثر مما أفادت في تطوير علاجات لهذا المرض".
ولتحقيق الاستفادة القصوى من هذه التقنية، يحتاج العلماء إلى إيجاد سُبُل يتسنَّى لهم من خلالها زراعة أجهزة أكثر تعقيدًا، عن طريق إضافة خلايا مناعية وأوعية دموية إلى العُضيَّات، على سبيل المثال. ويحتاج الباحثون أيضًا إلى تعزيز كفاءة عملية الإنتاج، لتخليق الآلاف، بل والملايين، من العُضيَّات المتطابقة بسرعة كبيرة، وبتكلفة زهيدة.
وتقول جي جو، عالمة الفيروسات في جامعة هونج كونج: "لا يزال استخدام العُضيَّات المستزرعة في دراسة الفيروسات في مراحله الأولى".
فيروسات لا يمكن استزراعها
قبل أن تبدأ عالمة الفيروسات ماري إستس في استخدام تقنية العُضيَّات، كانت تعتمد على طريقة أكثر تعقيدًا لدراسة «فيروس نورو» norovirus، المعروف بسرعة انتشاره، ويُشار إليه أيضًا باسم «حشرة القيء». لم يستطع الباحثون من قبل استزراع الفيروس في المختبر، ولذا لجأت إستس إلى عزل الفيروس من براز أشخاص ابتلعوا الفيروس طواعيةً – وعانوا تبعات ابتلاعه – في سبيل إجراء بحثها.
اطَّلعت إستس في عام 2011 على بحثٍ أجراه كليفرز، حيث استنبت أمعاء مصغَّرة من خلايا جذعية كُشِطت من الزُّغابة المعوية؛ وهي مجسَّات مجهرية تُبطِّن أمعاء الإنسان1. استنبت كليفرز أول عُضيَّات مُشتقة من خلايا جذعية بالغة، تنمو لأجَل غير مسمًّى تقريبًا، إذا ما توفرت لها ظروف النمو المناسبة، وبمقدورها أن تنمو بحيث تكوِّن بِنًى معقَّدة تتخذ شكل العضو الأصلي الذي أُخذت منه. (كانت العُضيَّات قد استُنبتت بالفعل في السابق من خلايا جذعية جنينية، أو خلايا جذعية مستحثَّة متعددة القدرات (iPS)، وهي خلايا يمكن أن تنمو مكوِّنةً أي نوع من الخلايا، لكنها تتخذ عادةً شكل الأعضاء في المراحل الأولى من تطور الأجنّة).
تقول إستس، الأستاذ بكلية بايلور للطب في مدينة هيوستن بولاية تكساس: "قلت لنفسي إنّه ربما يتعيَّن علينا تجربة هذا النظام؛ فلم يكن هناك من أحدٍ يستخدم تلك الخلايا المستنبتة في علم الفيروسات في ذلك الوقت".
وفي عام 2016، أي بعد انقضاء قرابة نصف قرن على اكتشاف فيروس «نورو» الذي يصيب الإنسان، كانت إستس أول من استنبت الفيروس في طبق مخبري بطريقة تتيح تكاثره في عُضيٍّ معوي2.
وقد أثبتت أبحاثها أن العُضيَّات المستزرعة تُمثِّل نموذجًا جيدًا للأمراض التي تصيب البشر. فقد اكتشفت إستس، على سبيل المثال، أن سلالات فيروس «نورو» لم تتكاثر في جميع العُضيَّات التي استُنبتت من خلايا لأشخاص لا تظهر عليهم – في المعتاد – أية أعراض من جراء الإصابة بهذا الفيروس2.
ومنذ ذلك الحين، يستخدم الباحثون العُضيَّات لدراسة مزيد من الفيروسات، التي تشمل «الفيروس التنفسي المخلوي» RSV – الذي يُسبِّب عدوى تنفسية لدى الأطفال – في عُضيَّات المجرى التنفسي، وفيروس «بي كيه» BK الغامض والنادر في عُضيُّات الكُلَى.
وفي عام 2016، حَقَن فريق من الباحثين عُضيَّات دماغ في طور النمو بفيروس «زيكا» Zika، وأثبتوا أن ثمة ارتباطًا بين إصابة السيدات الحوامل بهذا الفيرو، وما يُعرف بالصَّعَل3 الذي يشير إلى حالة يكون فيها رأس الجنين أصغر من الحجم الطبيعي. فبعد 10 أيام من الإصابة بالعدوى، تبيَّن أن حجم عُضيَّات الدماغ يكون أصغر بنسبة 40% من العُضيَّات التي لم تُصب بالفيروس. وتقول باترشيا جارسيز، اختصاصية البيولوجيا العصبية في الجامعة الفيدرالية في ريو دي جانيرو بالبرازيل، التي قادت الفريق البحثي، إنّ هذه الخلايا السَّلَفية العصبية هي بمثابة "بيئة خصبة لعدوى فيروس زيكا".
وفي عام 2018، طوَّر كليفرز وجو وزملاؤهما عُضيَّات رئة، يمكن الاستعانة بها في إجراء تقييمٍ سريعٍ لمدى انتشار عدوى أحد فيروسات الإنفلونزا الجديدة4. فبعض السلالات المعروفة بشدة انتشارها بين البشر، ومنها فيروس«إتش 1 إن 1» H1N1، الذي تسبَّب في انتشار وباء إنفلونزا الخنازير في عام 2009، كان تتكاثر في العُضيَّات على نحو أسرع من تكاثر السلالات التي عادةً ما تصيب الخنازير والطيور.
وفضلًا عن هذه الأمثلة، أجرى عددٌ قليلٌ من علماء الفيروسات أبحاثهم على العُضيَّات المستزرَة مخبريًا عندما ظهر فيروس «سارس-كوف-2»، واستحوذ على اهتمامهم.
وسرعان ما أدرك كليفرز الإمكانات الكبرى التي تنطوي عليها نماذج العُضيَّات في دراسة فيروس غريب، في خضم جائحة عالمية. يوضح كليفرز أنه كانت هناك دلالات واضحة من الأبحاث الإكلينيكية تُفيد بأن الفيروس يمكن أن يؤثر على الأمعاء، خصوصًا لدى الأطفال، وهو ما جعله يتساءل عما إذا كان بمقدوره استخدام عُضيَّات الأمعاء لتحديد مدى قدرة الفيروس على إصابة النسيج المعوي بالعدوى.
وفي الخامس عشر من شهر مارس عام 2020 – وهو اليوم الذي قررت فيه هولندا تطبيق قرار الإغلاق – طلب كليفرز من زملائه في مدينة روتردام عيناتٍ من فيروس «سارس-كوف-2». وبعد مُضي عدة أسابيع، نشر هو وزملاؤه بحثًا في مجلة «ساينس» Science، أوضحوا فيه أن فيروس «سارس-كوف-2» تكاثر بسرعة في نماذج الأمعاء المُصغَّرة، وأنه استهدف بالأخص خلايا تُعرف باسم خلايا الامتصاص المعوي (enterocytes)، التي تُبطِّن الأمعاء5 وقد ساعدت هذه الدراسة على كشف السبب الذي يجعل بعض المصابين بعدوى «كوفيد-19» يعانون من مشكلات في الجهاز الهضمي، تشمل الإسهال والقيء، ومن ثم وقفَتْ على طريقٍ آخرَ محتملٍ لانتقال العدوى.
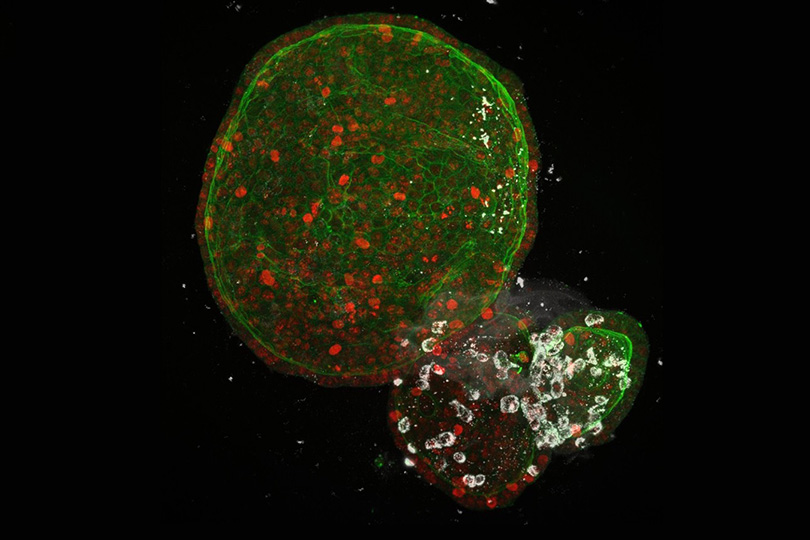
ومنذ ذلك الحين، أثبت الباحثون أن فيروس «سارس-كوف-2» لديه القدرة على إصابة مجموعة من الأعضاء المُصغَّرة (من الكبد إلى الكُلى إلى الدماغ)، على نحوٍ يحاكي الضرر الذي يصيب عدة أعضاء، والذي رُصد لدى بعض المصابين بمرض «كوفيد-19»، (انظر الشكل: أعضاء في طبق مخبري).
ولأسبابٍ وجيهة، حظيت الرئة بنصيب الأسد من اهتمام الباحثين. ففي عُمق الرئة، توجد أكياس هوائية دقيقة تُعرف باسم الحويصلات الهوائية، وهي موضع الالتهاب الرئوي لدى الأشخاص الذين يتعرَّضون لإصابة حادة بمرض «كوفيد-19». ونظرًا إلى صعوبة وصول الباحثين إلى هذه الخلايا ودراستها، فقد لجأت كاترين بليش، اختصاصية المناعة الفيروسية في جامعة ستانفورد بولاية كاليفورنيا، بمعاونة فريقها، إلى الخلايا التي تكوِّن تلقائيًّا هذه الأكياس الهوائية، لبحث كيفية حدوث العدوى.
وقد توصَّل الباحثون إلى أن الفيروس ألحق ضررًا بالغًا بالعُضيَّات المستنبَتة من الحويصلات الهوائية، ومن الخلايا الموجودة في الممرات التنفسية الدقيقة التي تُغذيها6. ففي الحويصلات الهوائية، استهدف فيروس «سارس-كوف-2» الخلايا التي تغطي السطح المعرَّض للهواء، والتي تحتوي على كميةٍ وفيرة من «مستقبِل الإنزيم المحوِّل للأنجيوتنسين-2» ACE2، الذي يستعين به فيروس «سارس-كوف-2» في النفاذ إلى الخلية. وقد أصاب الفيروس أيضًا الخلايا المضربية الموجودة في الممرات الهوائية، التي تفرز جزيئًا بهدف التعامل مع التمدد المستمر في الرئتين. تقول بليش: "بفضل العُضيَّات، أصبح في إمكاننا معرفة أن الخلايا المضربية يمكن أن تُعزِّز تكاثر فيروس «سارس-كوف-2»؛ لأنّ أحدًا لم يخطر بباله أن الفيروس يحطُّ على الخلايا المضربية".
استطاعت دراساتٌ أخرى، أُجريت على الحويصلات الهوائية المُصغَّرة، الكشف عن تفاصيل الاشتباك الذي يحدث بين الفيروس والخلايا7. فقد وجد يونج سونج جو، اختصاصي علم جينوم في المعهد الكوري المتقدّم للعلوم والتكنولوجيا في مدينة دايجون، أن الخلايا تستغرق يومًا كاملًا تقريبًا كي تُصْدِر استجابةً. يعقُب ذلك صراع بين الخلايا والفيروس، واعتبارًا من اليوم الثالث، يبدأ في الفتك بأكثر من ربع الخلايا.
يتطلع العلماء كذلك إلى معرفة المزيد عن كيفية نفاذ الفيروس إلى داخل الخلايا. ففي إحدى الدراسات، استخدم الباحثون تقنية التحرير الجيني «كريسبر» CRISPER في عُضيَّات الأمعاء، بهدف الكشف عن بروتينَين آخرين (هما: TMPRSS2، وTMPRSS)، يُسهمان مع مستقبِل ACE2 في تسهيل دخول الفيروس إلى الخلية8 ويعمل باحثون في مختبراتٍ أخرى على تعطيل المستقبِل ACE2 تمامًا، كي يتبينوا ما إذا كان الفيروس سينجح في دخول الخلية في غيابه. تقول شين: "كلما تعمّقنا في دراسة العُضيَّات، أصبحنا أكثر وعيًا بأن الأنواع المختلفة من الخلايا تتّبع آلياتٍ مختلفة في تعزيز قدرة الفيروس على دخول الخلية".
استُخدمت العُضيَّات أيضًا في دراسة السلالات المتحوِّرة من فيروس «سارس-كوف-2». ففي نسخةٍ أولية لأحد الأبحاث، درس كليفرز - بالتعاون مع زملائه - عُضيَّات المجرى الهوائي والحويصلات الهوائية والأمعاء لدى البشر، ووجدوا أن المتحوِّر B.1.1.7، الذي رُصد للمرة الأولى في المملكة المتحدة، قادرٌ على إنتاج كميات أكبر من الفيروس المُعدي في مراحل متأخرة من العدوى، مقارنةً بالمتحوِّرات المنتشرة من قبل9 ولعل ذلك يُفسر سبب زيادة انتشار هذه السلالة المتحوِّرة.
لَوْزات مُصغَّرة
إنّ نجاح الباحثين في رصد الفيروس بدقة وهو يفتك بخلايا الجسم قد يساعد الباحثين على تحديد سبل السيطرة عليه. يشير أرينجاي بانيرجي، الباحث المتخصص في فيروس كورونا في جامعة ساسكاتشوان الكندية، الذي يعتزم استخدام عُضيَّات الأمعاء في أبحاثه، إلى أن العُضيَّات تساعد على سدِّ الفجوة بين مراقبة الفيروس في مجموعات الخلايا التي تفتقر إلى التعقيد الذي يميز الأنسجة الحقيقية، ومراقبته في النماذج الحيوانية التي تعطي صورة قاصرة عن العدوى لدى الإنسان، فضلًا عن تكلفتها المرتفعة.
وتقول بليش إن الكثير من العقاقير المرشَّحة، التي تبدو واعدةً في صفائح الخلايا، غالبًا ما يكون مآلها الفشل في مراحل لاحقة. ومن بين الأمثلة الواضحة على ذلك، عقار «هيدروكسي كلوروكين» hydroxychloroquine، وهو أحد أوائل العقاقير التي اعتُبرَتْ علاجًا لمرض «كوفيد-19» في بداية الجائحة. فقد أشارت الدراسات التي أُجريت على خلايا «فيرو» إلى أن الكلوروكين يمكن أن يمنع نفاذ الفيروس إلى الخلايا، إلا أن التجارب الإكلينيكية اللاحقة أثبتت أنه لا يوفِّر الحماية المزعومة. درس كليفرز، وغيره من الباحثين، آلية إصابة عُضيَّات الأمعاء بعدوى فيروس «سارس-كوف-2»، ليجدوا أن الطريق الذي سلكه الفيروس للدخول إلى هذه العُضيَّات كان مختلفًا عن الطريق الذي سلكه لإصابة خلايا «فيرو»، واكتشفوا أن عقار «هيدروكسي كلوروكين» يمكن أن يمنع دخول الفيروس إلى خلايا «فيرو»، لكنه لا يمنع دخوله إلى العُضيَّات10 يقول كليفرز: "لو كانت اختبارات تلك العقاقير الأولى أُجريت على العُضيَّات، بدلًا من خلايا «فيرو»، لما اعتُبر عقار «كلوروكين» أحد العلاجات المرشَّحة من الأصل".
يسعى كثيرٌ من الباحثين إلى الاستفادة من إمكانات العُضيَّات في اكتشاف العقاقير. وقد اختبرت شين نحو ألف عقار على القولونات والرئات المصغّرة، وحدَّدت سبعة منها، بدا أنها تحمل نتائج واعدة11 من بينها عقار «ريمديسيفير» remdesivir المضاد للفيروسات، الذي تبيَّن بالفعل أنه حقق شيئًا من الفائدة للمشاركين في التجارب الإكلينيكية. وترى شين أن النتائج التي توصلت إليها إنما هي دليل على جدوى اختبار الأدوية على العُضيَّات.
والاختبار الذي ضمَّ 15 ألف عقار يُعَد أكبر المحاولات التي نفَّذتها شين إلى الآن. فقد قضت أسابيع تعدِّل أساليب عملها لتخليق عُضيَّات متماثلة قدر الإمكان. وتقول في هذا الشأن: "دائمًا ما يكون التباين بين العُضيَّات، والمقارنة غير المتكافئة، مبعث قلقٍ لنا". وتُضيف قائلة إنّ هذا الاختبار يندرج تحت مظلة مشروع أكبر، تَستخدم فيه عدة مختبرات آلياتٍ مختلفة لدراسة المركبات نفسها، ومقارنة نتائجها لاحقًا.
استُخدمت العُضيَّات أيضًا في اختبار اللقاحات. ففي يناير من العام الجاري، استنبت باحثون لوزات مُصغَّرة من أجزاء صغيرة من نسيجٍ تم الاستغناء عنه خلال إحدى العمليات الجراحية. واللوزات معروفة بدورها المحوري في الدفاع عن الجسم؛ فهي عادةً ما تكون أول عضو ينتج خلايا مناعية للتصدي للعامل المُمرِض، لضمان توفير حماية طويلة الأمد.
وعندما أضاف الباحثون أحد اللقاحات المرشَّحة للتصدي لمرض «كوفيد-19» إلى عُضيَّات اللوزات، كَوّن بعضها استجابة مناعية عن طريق إنتاج «الخلايا التائية» T cells القاتلة، إضافة إلى أجسامٍ مضادة قادرة على استهداف البروتين الشوكي على سطح الفيروس12. لكنْ لا تزال الحاجة قائمة لإجراء الكثير من الأبحاث، بهدف التوثُّق مما إذا كان ما يحدث في الأطباق المخبرية هو نفسه الذي يحدث في جسم الإنسان.
إضافةً إلى ذلك، فإن أعضاء الجسم لا توجد بمعزل عن بعضها البعض. ولفهْم ما يحدث عندما يصاب الإنسان بعدوى فيروس «سارس-كوف-2»، ومعرفة ما إذا كانت العلاجات المرشَّحة ناجعة أم لا، يحتاج الباحثون إلى أجهزةٍ أكثر تعقيدًا تحتوي على خلايا مناعية، وخلايا أوعية دموية.
وفي دراسة لم تُنشر بعد، زرع تاكانوري تاكيبي، العالِم الإكلينيكي واختصاصي بيولوجيا الخلايا الجذعية في جامعة طوكيو للطب وطب الأسنان، خلايا أوعية دموية في عُضيَّات الكبد، ليجد أن الشعيرات الدموية والأوردة الأصغر حجمًا تكون أكثر عُرضة للإصابة بفيروس «سارس-كوف-2»، مقارنةً بالأوعية الدموية الأكبر حجمًا. أما شين، فقد زرعت خلايا مناعية تُعرف باسم «البلعميات الكبيرة» على صفائح من خلايا عضلة القلب13 وهي تفعل الشيء نفسه حاليًّا مع عُضيَّات الرئة التي تُخضِعها للبحث. ومن الممكن أن تساعد هذه التجارب، جنبًا إلى جنب مع الدراسات التي تُجرى على النماذج الحيوانية، في حسم الجدال المستمر عن السبب وراء هذا الارتفاع في نسبة الوفيات بين مرضى «كوفيد-19»؛ أهو الفيروس نفسه، أم فرط الاستجابة المناعية التي يستحثها؟
في التصوُّر المثالي، يطمح الباحثون إلى ربط العُضيَّات معًا، إذ يمكن لهذه الأجهزة أن تكشف، مثلًا، كيفية تأثير العدوى – التي تبدأ في الرئة – على القلب أو الأمعاء. تقول مولبرجر: "يتطلع علماء الفيروسات جميعًا إلى توافر أعضاء مختلفة، ومتصلة بعضها ببعض. فكلما اقتربنا من الأعضاء البشرية، كان ذلك أفضل، واستطعنا معرفة السر وراء قدرة الفيروسات العالية على الإمراض".
في عام 2019، ربط تاكيبي بين عُضيَّات كبد، وقناةٍ صفراوية، وبنكرياس14 لكنْ لم ينشر أي فريق بحثًا إلى الآن باستخدام نماذج تتضمن عدة أعضاء لدراسة فيروس «سارس-كوف-2».
الجائحة القادمة
من المُرجَّح أن تمتد العلاقات التي تشكَّلت بين علماء البيولوجيا الخلوية وعلماء الفيروسات لما بعد جائحة «كوفيد-19».
في مقابل كل عُضيَّة حَقَنَتْها مولبرجر بفيروس «سارس-كوف-2»، أجرت تجربةً موازية باستخدام فيروس «إيبولا»، الذي يُسبِّب حمَّى نزفية قاتلة، لا يوجد لها سوى نماذج قليلة للغاية من العدوى. وقد وجدت مولبرجر أن فيروس «إيبولا» يمكن أن يصيب جميع الأنسجة تقريبًا؛ بل هو قادرٌ على الوصول إلى أماكن لا يستطيع فيروس «سارس-كوف-2» الوصول إليها. وهذه القدرة، في رأيها، هي ما تجعل فيروس «إيبولا» قاتلًا إلى هذ الحد.
وفيما يخص التنبؤ بالجائحة القادمة، فإن بعض الباحثين يتجهون الآن إلى العُضيَّات المأخوذة من خلايا حيوانية.
ففي مطلع عام 2020، تواصلت جُو مع شي تشنج-لي، عالمة الفيروسات في معهد ووهان لأبحاث الفيروسات في الصين، التي ساعدتها على التعرُّف على أقرب سلالة لفيروس «سارس-كوف-2»، وهي فيروس كورونا RATG13، الذي يصيب الخفافيش. قالت شي إنها عيَّنت التسلسلات الجينومية لمئات من فيروسات كورونا من الخفافيش، لكنها لم تتمكن سوى من زراعة عدد قليل منها. وقد تساءلت جُو عما إذا كان بإمكانها زراعة عُضيَّات من أنسجة الخفافيش؛ إذ يمكن استخدام هذه العُضيَّات في اختبار العقاقير التي يمكن أن تستهدف مجموعةً واسعة من الفيروسات التي لديها القدرة على إصابة الإنسان بالعدوى.
اقتطعت جُو أجزاءً صغيرة من أمعاء خفافيش حدوة الحصان Rhinolophus sinicus، وعملت على استنبات أمعاء خفافيش مُصغَّرة من عدة أنواع من الخلايا. وقد نما فيروس «سارس-كوف-2» بشكلٍ جيد على الأمعاء15، وهو ما يُعَد أول دليل تجريبي على أن فيروس كورونا يمكن أن يصيب خفافيش حدوة الحصان، وهذا بدوره يدعم الفرضية القائلة بأنّ أصل الفيروس إنما يعود إلى الخفافيش.
لا يزال نهج دراسة الفيروسات باستخدام العُضيَّات يقطع أولى خطواته، غير أن قسمًا كبيرًا من الباحثين يعتبرون هذا النهج نموذجًا مهمًّا لدراسة التفاعلات بين الخلايا البشرية والفيروسات. وتشير جُو إلى أن هذه التقنية قد تجعل الاستجابة للجائحة القادمة أسرع، وأكثر كفاءة، تقول إستس: "إنها تقنية مذهلة، وليس في إمكان أحد أن يتصور الآفاق التي قد تفتحها لنا في هذا المجال".



اضف تعليق